Миеломная болезнь (плазмоцитома)
Содержание:
- Общие сведения
- Диагностика миеломной болезни
- Прогнозировование и факторы риска при миеломе
- Общие принципы терапии
- Причины миеломной болезни
- Прогноз и шансы на выживаемость по стадиям
- Часто задаваемые вопросы
- Симптоматика миеломной болезни
- Миеломная болезнь – симптомы
- Анемия
- Суть заболевания
- Симптомы миеломной болезни
Общие сведения
Итак, миелома крови берет свое начало в костном мозге, после чего патологический процесс распространяется дальше по всему организму. Первые признаки болезни – болевой синдром в костях, так как в этой зоне образуется злокачественная опухоль. У больного также возникает нарушение функционирования опорно-двигательного аппарата, особенно при тяжелом течении болезни.
Каждый больной должен понимать, что в настоящее время ученые не могут установить точные причины возникновения заболевания. Но выявили статистику, что склонны к такому недугу те люди, которые перенесли радиацию или длительное время находились с нефтеперерабатывающими продуктами. Как правило, болезнь возникает после 40 лет, в молодом возрасте встречается редко.
При миеломе, назначают анализ крови и инструментальные методы диагностики. Только так можно быстро определить течение болезни. Теперь вы понимаете, что это такое. Рассмотрим основные провоцирующие факторы, которые приводят к данному недугу.
Диагностика миеломной болезни
Лабораторная диагностика и скрининг парапротеинемий основан на выявлении «парапротеина» крови. Очень чувствительным методом диагностики парапротеинемий является иммунофиксация белков сыворотки и мочи с панелью антисывороток IgG, IgM, IgA, IgE, IgD, каппа, лямбда. Диагностическая значимость обнаружения парапротеинемии значительно увеличивается при характерной клинике, указывающей на плазмаклеточное заболевание. При скрининге лиц без симптомов методом электрофореза или иммунофиксации в отсутствии клинических проявлений миеломы обнаружение парапротеина указывают на моноклональную гаммапатию невыясненного значения (МГНЗ). К клиническим показаниям для исследования парапротеина относят боли в костях, патологические переломы, полинейропатию, лихорадку, анемию. Для парапротеинемий характерны такие лабораторные находки, как увеличение скорости оседания эритроцитов, протеинурия и азотемия, гиперкальцемия, увеличение содержания общего белка сыворотки, а также отклонения от нормы в содержании основных белковых фракций. Инфекционные процессы также часто сопутствуют миеломе, поскольку синтез парапротеина подавляет синтез нормальных иммуноглобулинов, что ведет к нарушению функций иммунной системы. Иммунохимическое исследование основных иммуноглобулинов сыворотки крови IgG, IgA, IgM позволяет выявить изменение их синтеза. Однако при оценке парапротеинемий иммунохимическое определение иммуноглобулинов не рекомендовано в связи с частым феноменом «прозоны» при высоких концентрациях и неточностью измерения моноклональных молекул, поскольку особенности синтеза в миеломной клетке меняют антигенные свойства иммуноглобулинов. Во всех этих случаях методом выбора для выявления и измерения парапротеина является электрофорез с иммунофиксацией белков сыворотки и мочи. Парапротеин представлен иммуноглобулином IgG примерно у половины больных, IgA — у 20%, IgD — у 2%, IgM — у 0.5%. У 20% больных парапротеин представлен только свободными цепями иммуноглобулина. В 2-3% случаев заболевания парапротеин не определяется, что рассматривается как несекретирующая миеломная болезнь. Если быть точным, это название не соответствует действительности, поскольку при несекретирующей миеломе можно обнаружить свободные легкие цепи в сыворотке крови или моче. Диагностическая панель из сочетания электрофореза сывороточного белка, сывороточной иммунофиксации и определения свободных легких цепей в сыворотке или электрофореза с иммунофиксацией в образце 24 часовой мочи рекомендована всем лицам с подозрением на миеломную болезнь. Чувствительность обнаружения моноклональных белков равняется в среднем 82% для электрофореза белков, 93% для иммунофиксации и 97% при добавлении результатов свободных легких цепей или электрофореза белка и иммунофиксации в образце 24-часовой мочи. Отсутствие моноклонального белка примерно у 2% больных типично для несекретирующей миеломной болезни.
В подавляющем числе случаев диагностика миеломной болезни начинается после появления характерной симптоматики. Диагноз миеломной болезни после появления таких симптомов, как повышенная утомляемость и боли в спине на практике обычно запаздывает на срок свыше 3 месяцев. Хотя неизвестно, как это сказывается на исходе заболевания в целом, но частота осложнений и госпитализаций за этот период отсрочки возрастает, что негативно влияет на качество жизни больных. Многие факторы влияют на причину задержки, включая неспецифический характер жалоб и расстройств, которые нередко наблюдаются у лиц пожилого возраста и которые первоначально рассматриваются ими и их родственниками как доброкачественные. Но устойчивый характер болей в позвоночнике и повышенной утомляемости должен всегда настораживать практических врачей. Обследование по поводу мышечно-скелетных болей, анемии, тромбоцитопении, почечной недостаточности, гиперкальциемии, неврологических расстройств может привести к обнаружению моклонального белка в сыворотке или моче.
Кроме того, диагностический поиск миеломной болезни включает полный подсчет клеток крови и СОЭ, измерение уровня сывороточного кальция и креатинина, электрофорез белков сыворотки и мочи с иммунофиксацией, исследование свободных легких цепей в крови, исследование пунктата костного мозга. Дополнительно, низко-дозная КТ всего тела или ПЭТ с 18-флюородезоксиглюкозой/ КТ или ,как минимум, обзорная рентенография всего скелета требуется для выявления остеолитических поражений костей.
Прогнозировование и факторы риска при миеломе
«Международная система прогнозирования» (ISS. 2005) была разработана на основании данных естественного исхода заболевания значительной клинической группы больных и основана на исследовании бета-2 микроглобулина в динамике. Бета-2 микроглобулин повышен у 75% больных миеломной болезнью.
Выделено три уровня этого онкомаркера, которые связаны с длительной выживаемостью пациентов. Это позволяет определить несколько стадий заболевния.
- бета-2-микроглобулин менее 3,5 мг/л и альбумин более 35 г/л, средняя выживаемость 62 месяца,
- промежуточная между 1 и 3 стадиями, средняя выживаемость 44 месяца.
- бета 2-микроглобулин более 5.5 мг/л, средняя выживаемость 29 мес.
Однако, в настоящее время использование новых препаратов значительно изменило прогноз естественного течения заболевания. Тем не менее, международная система была протестирована для новейшей терапии и подтвердила свою надежность. Так, 5-летняя выживаемость больных в стадии I, II и III составила 66%, 45% и 18% соответственно.
В Международной системе не оказалось места для таких ценных прогностических показателей как число тромбоцитов, уровень лактатдегидрогеназы и свободных легких цепей в крови.
Число тромбоцитов в крови коррелирует с вытеснением костного мозга и имеет предсказательное значение выше, чем у альбумина. Содержание лактатдегидрогеназы (ЛДГ) коррелирует с общей массой миеломных клеток, недостаточным ответом на терапию и укорочением выживаемости. У больных с уровнем свободных легких цепей в крови свыше 4,75 г/л чаще выявляется почечная недостаточность, высокой процент миеломных клеток в пунктате костного мозга, высокие значения бета-2-микроглобулина и лактатдегдрогеназы, чаще обнаруживается болезнь отложения легких цепей и стадия III по Международной системе. Однако представленных доказательств оказалось недостаточно, чтобы включить эти три критерия в Международную систему. Но они были представлены в системе Дьюри-Саймона (1975), значение которой не оспаривается до сих пор.
Повышенный уровень сывороточного бета 2-микроглобулина, повышенный уровень лактатдегидрогеназы и низкий уровень сывороточного альбумина относятся к неблагоприятным признакам прогноза при миеломной болезни. Хотя уровень бета-2- микроглобулина увеличивается при почечной недостаточности, существует значительная корреляция между объемом опухолевой ткани и концентрацией этого биомаркера в крови. Исключение составляют лишь случаи, когда миеломная болезнь развивается уже на фоне имеющейся почечной недостаточности.
Перспективным методом оценки прогноза заболевания является генетическое исследование опухоль-ассоциированных генов. Цитогенетическое выявление транслокаций в отличие от трисомии относится к неблагоприятным прогностическим признакам. Метод флюоресцентной гибридизации in situ (FISH) позволил упростить выявление хромосомных аберраций в миеломных клетках, что предлагается исследователями клинико Мэйо (США) использовать для выбора индивидуальной лечебной тактики, исходя из прогноза для больного на основании учета выявленных аберраций. Генетические исследования хромосомных аномалий и мутаций при миеломе являются перспективными методами для лабораторной оценке прогноза и устойчивости к терапии при миеломе. Однако для их оценки требуются большие сроки и число пролеченных больных, чтобы определить способность новых средств терапии преодолеть цитогенетические показатели высокого риска при миеломной болезни.
Общие принципы терапии
Лечение миеломы не предусматривает применения радикальных методов, так как основной задачей курса терапии является продление и улучшение качества жизни. Вылечить полностью миелому невозможно. Однако в борьбе с опухолевым поражением можно затормозить его развитие и вызвать ремиссию.
После точного диагностирования миеломной болезни, лечение проводится с использованием паллиативных методов, позволяющих затормозить рост новообразования и ослабить признаки. К паллиативным способам лечения миеломы относится химическая терапия, облучение и подбор правильного питания. Проводить лечение народными средствами в домашних условиях не рекомендуется.
Рекомендуем к прочтению Гемангиома на лице у детей и взрослых — диагностика, лечение, прогноз
Химиотерапия
Применение химиотерапии — самый результативный метод борьбы с миеломой. Во время проведения курса лечения может использоваться как один препарат (монохимиотерапия), так и несколько медикаментозных средств (полихимиотерапия).
При назначении полихимиотерапии могут использоваться следующие препараты:
- Циклофаосфамид;
- Мелфан;
- Леналидомид;
- Дексаметазон.

Препараты принимают внутрь или внутривенно с помощью внутримышечных инъекций. Когда назначают курс химиотерапии, лечение может проводиться по одной из нескольких схем:
- Схема MP — прием препаратов мелфалан и преднизолон в таблетированном виде.
- Схема M2 — введение внутривенных инъекций винкристина, циклофосфамида и BCNU. Вместе с этим на протяжении двух недель необходимо принимать таблетки преднизолона и мелфалана.
- Схема VAD — терапия проводится в 3 сеанса. Во время первого сеанса лечение проводится лекарствами доксирубицин и винкристин. Во время следующих сеансов необходимо принимать таблетки дексаметазона.
- Схема VBMCP — назначается больным, возраст которых младше 50 лет. В первый день терапии пациентам внутривенно вводят винкристин, циклофосфамид и кармустин. Затем на протяжении недели необходимо пить мелфалан и преднизолон. Через полтора месяца им вновь вводят инъекцию кармустина.

После лечения химиопрепаратами стойкая ремиссия наблюдается у 40% пациентов.
Лучевая терапия
Применение лучевой терапии назначается обычно при солитарных и крупноочаговых опухолях, когда лечение химиопрепаратами бессильно. В таком случае удается затормозить развитие злокачественного образования и ослабить клинические проявления болезни.
Если облучение и применение химических препаратов не дали эффекта, пациентам проводят пересадку костного мозга. Примерно у 40% пациентов трансплантация стволовых клеток помогает достичь стойкой ремиссии болезни.
Симптоматическое лечение
Этот способ лечения множественной миеломы предполагает прием назначенных лекарств. Их действие направлено на купирование болей, корректировку концентрации кальция в крови. Препараты нормализуют свертываемость крови и стабилизируют работу почек.
Иногда еще возможно проведение операции по удалению одиночного очага миеломы, над которым потом проводится цитологическое исследование. Если наблюдается тяжелое течение болезни, пациентам может быть назначено применение морфина, бупренорфина и других наркотических препаратов.
Питание

Во время лечения болезни обязательно нужно придерживаться правильного питания. Диету при миеломной болезни назначает лечащий специалист. В рационе следует ограничить употребление продуктов с большим содержанием белка. Больному нужно есть меньше мясных блюд, яиц, бобовых и орехов.
Причины миеломной болезни
Болезнь Рустицкого-Калера изучена врачами, однако по поводу причин ее возникновения в медицинских кругах нет единого мнения. Было обнаружено, что в организме больного человека часто присутствуют лимфатические вирусы Т или В типа, а поскольку из В-лимфоцитов образуются плазмоциты, любое нарушение этого процесса приводит к сбою и началу образования патоплазмацитов.
Помимо вирусной версии, имеются доказательства того, что миеломная болезнь может быть спровоцирована и в результате радиоактивного облучения. Врачи изучали людей, пострадавших в Хиросиме и Нагасаки, в зоне взрыва на Чернобыльской АЭС. Было обнаружено, что среди получивших большую дозу облучения высок процент заболевших миеломой и другими заболеваниями, поражающими кровеносную и лимфатическую системы.
Среди негативных факторов, которые повышают риск заболеть миеломной болезнью, врачи называют:
- курение – чем дольше стаж курильщика и больше количество выкуриваемых сигарет, тем выше риск;
- иммунодефицит;
- воздействие на организм токсичных веществ;
- генетическую предрасположенность.
Прогноз и шансы на выживаемость по стадиям
Для обозначения тяжести протекания заболевания, как и другие болезни, миелома подлежит стадированию. Именно стадия определяет не только дальнейшую терапию, но и прогноз заболевания. Чем раньше диагностировать болезнь, тем быстрее можно начать лечение и, как следствие, ускорить процесс ремиссии.
К сожалению, на первой стадии, когда существуют все шансы успешного лечения, диагностировать заболевание практически невозможно. Пациент может длительное время не догадываться о наличии болезни, т.к. она зачастую протекает бессимптомно. Только отклонения в общих анализах крови, а именно повышенная СОЭ, может свидетельствовать о начальном этапе онкологии. 50% больных миеломой, которые обнаружили заболевание на первой стадии развития доживают до 5 лет.
На второй стадии заболевание начинает прогрессировать и проявлять себя различными симптомами, такими как: беспричинные боли в костях, которые практически не устраняются обезболивающими препаратами, постоянная усталость, анемия, нарушение зрения. Данный этап также довольно трудно диагностируется, т.к.
Часто задаваемые вопросы
Как я могу попасть на консультацию к онкологу?В какое время принимают онкологи?В какие часы проводится обследование и лечение?На каком языке проходит консультация?В LISOD лечат детей?Можно, я буду не один/одна на консультации?Как подготовиться к первой консультации?Что нужно знать при обращении в LISOD?Существует ли возможность консультации без пациента, только по документам?Сколько врачей будут наблюдать меня?Как подготовиться к проведению исследований?Существуют ли программы для профилактики возникновения рака?Оформляете ли вы приглашение на консультацию для граждан других стран?В LISOD проводят все виды лечения?
Симптоматика миеломной болезни
Симптоматику миеломы делят на 2 группы. Это:
- признаки, которые связывают с прогрессированием злокачественной опухоли в костном мозге;
- симптомы, которые присущи распространению опухоли в разных областях организма, а также попаданием парапротеинов в кровоток.

Клиника и симптомы множественной миеломы
Клиническая картина миеломной болезни, которая прогрессирует в костной ткани такова.
| Симптом | Из-за чего проявляется |
|---|---|
| Сильные, порой невыносимые боли в костях и суставах. Не локализуются в одной области, а наблюдаются по всему организму. Беспокоят преимущественно в ночное время и усиливаются при смене положения тела, чихании, кашле, любом движении | Боль в костях – это первый симптом, который отмечается при миеломной болезни. Имеет непостоянный характер |
| Множественные травмы, переломы, связанные с остеопорозом – повышенной ломкостью костей | Это заболевание обусловлено давлением опухоли на кости. Так, при сдавливании спинного мозга искривлёнными позвонками нарушается работа мочеполовой системы, кишечника, вследствие ухудшения нервной регуляции органов. В результате у больного отмечается диарея, проблемы с мочеиспусканием, недержание кала и другие нарушения |
| Мышечная слабость, потеря чувствительности ног | Появляются из-за сдавливания опухолью позвоночника |
| Рост больного становится заметно меньше | Это происходит вследствие деформирования костей |
| Переизбыток кальция в крови, или гиперкальциемия | Развивается достаточно медленно. Первыми симптомами гиперкальциемии являются: тошнота, невыносимая жажда, сухость во рту, обезвоживание, усталость, учащённое мочеиспускание, запор, похудение, мышечная слабость. Если вовремя не приступить к лечению заболевания, то это может привести к нарушению интеллектуальной деятельности, работы почек и коме |
| Анемия | Появляется характерная слабость и повышенная утомляемость. Прогрессирует вследствие вытеснения из костного мозга клеток-эритроцитов |
| Лейкопения | Уменьшение показателей лейкоцитов в крови. Болезнь становится источником резкого ослабевания иммунных функций. В связи с этим человек начинает страдать от разнообразных инфекций, вызванных воздействием вирусов и бактерий (менингит, грипп, воспаление лёгких) |
| Тромбоцитопения | Сокращение количества тромбоцитов в циркулирующей крови. Этот патологический процесс становится причиной плохой свёртываемости крови. В результате у больного наблюдаются гематомы, синяки, кровоточивость ран и десен. Часто человек просто не может остановить кровотечение |
| У больного нередко наблюдаются инфекции, вызванные воздействием бактерий | Это происходит по вине плазмоцитов, которые становятся источником снижения состава жизненно важных элементов в циркулирующей крови |

Проявления, механизм развития и симптомы миеломной болезни
Симптомы при опухоли в разных системах организма
Симптомы, которые присущи распространению опухоли в разных системах организма и попаданию парапротеинов в кровь.
- Плохая работа почек, недостаточность органа, развитие нефротического синдрома. Заболевания прежде всего связаны со скоплением в почках парапротеинов и регулярными инфекционными поражениями. В результате почки терпят колоссальную нагрузку, из-за чего орган источается, развивается недостаточность. Почечные поражения характеризуются наличием Бенс-Джонса белкового тела и мочевой кислоты в моче. Первый обнаруживается с помощью специализированного медицинского анализа. Присутствие в моче Бенс-Джонса белкового тела, как правило, и свидетельствует о развитии миеломы. В отличие от обычной почечной недостаточности, миеломная не сопровождается отёками и гипертонией.
- Нарушение свёртываемости крови. Развивается вследствие недостатка в крови тромбоцитов, а также их невозможности должно функционировать.
- Нарушения в сердечной работе (кардиомиопатия).
- Симптомы неврологических заболеваний.
- Увеличение селезёнки и печени в размерах.
- Повышенная густота крови. Сопровождается обильными влагалищными, носовыми, десенными, кишечными и другими кровотечениями. Кроме того, у больного отмечаются гематомы, синяки, ссадины. Ещё одним отличительным симптомом является «глаза енота». Для него характерно появление синяков под глазами после лёгкого прикосновения к данной области. Это обусловлено разрушением стенок сосудов и увеличенной густотой крови. Из-за плохого кровоснабжения на фоне миеломы у больного может развиться гипоксия, анорексия, сложные сердечные болезни.
- Разрушение ногтей, выпадение волос.
- Подвижность языка ухудшается, происходит его увеличение в размерах.
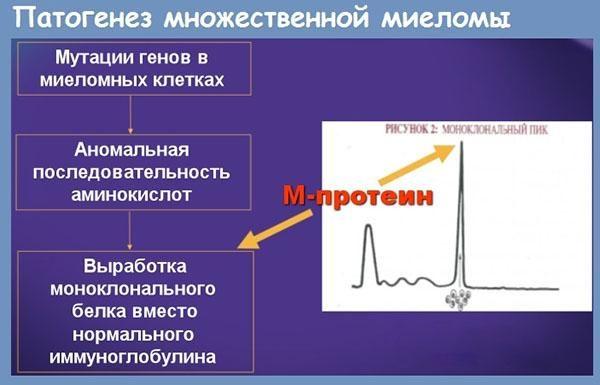
Патогенез множественной миеломы

Фазы миеломной болезни
Миеломная болезнь – симптомы
Миеломная болезнь преимущественно возникает в пожилом возрасте, поражая как женщин, так и мужчин. Болезнь Рустицкого-Калера – симптомы и клиническая картина, наблюдаемая у заболевших:
- поражение кроветворной и костной систем;
- нарушение обменных процессов;
- патологические изменения в мочевыделительной системе.
Множественная миелома симптомы:
- самые первые признаки миеломной болезни – боль в костях (в позвоночнике, грудной клетке, костях черепа), спонтанные переломы, деформация костей и наличие опухолевых образований;
- частые пневмонии и другие заболевания, спровоцированные падением иммунитета и ограничением дыхательных движений, вызванным изменениями в костях грудной клетки;
- дистрофические изменения в мышцах сердца, сердечная недостаточность;
- увеличение селезенки и печени;
- миеломная нефропатия – нарушение в почках с характерным повышением белков в моче, переходящее в почечную недостаточность;
- нормохромная анемия – снижение количества эритроцитов и уровня гемоглобина;
- гиперкальциемия – повышенное количество кальция в плазме и в моче, это состояние очень опасно, его симптомы – рвота, тошнота, сонливость, нарушения работы вестибулярного аппарата, психические патологии;
- снижение уровня нормального иммуноглобулина;
- нарушения кроветворения – кровоточивость слизистых, появление синяков, спазмы артерий фаланг, геморрагический диатез;
- парестезии («мурашки»), головные боли, сонливость, переходящая в ступор, судороги, головокружения, глухота, одышка;
- на последних стадиях – снижение веса, повышение температуры тела, серьезная анемия.

Формы миеломной болезни
По клинико-анатомической классификации миеломная болезнь бывает следующих форм:
- солитарная миелома – с одним опухолевым очагом в кости или лимфоузле;
- множественная (генерализованная) миелома – с формированием нескольких опухолевых очагов.
Кроме того, множественная миелома может быть:
- диффузной – в данном случае патологически образования не имеют границ, а пронизывают всю структуру костного мозга;
- множественно-очаговой – плазмоцитома кости развивается на ограниченных участках, а кроме этого, опухоли могут возникать в лимфатических узлах, селезенке.
- диффузно-очаговой – сочетающей признаки диффузной и множественной.
Миеломная болезнь – стадии
Врачи подразделяют три стадии множественной миеломы, вторая стадия является переходной, когда показатели выше, чем в первой, но ниже, чем в третьей (самой тяжелой):
- Первая стадия характеризуется – пониженным до 100 г/л гемоглобином, нормальным уровнем кальция, низкой концентрацией парапротеинов и белка Бенс-Джонса, одним опухолевым очагом размером 0,6 кг/м², отсутствием остеопороза, деформации костей.
- Третья стадия характеризуется – пониженным до 85 г/л и ниже гемоглобином, концентрацией кальция в крови выше 12 мг на 100 мл, множественными опухолями, высокой концентрацией парапротеинов и белка Бенс-Джонса, общим размером опухоли 1,2 кг/м² и более, явными признаками остеопороза.
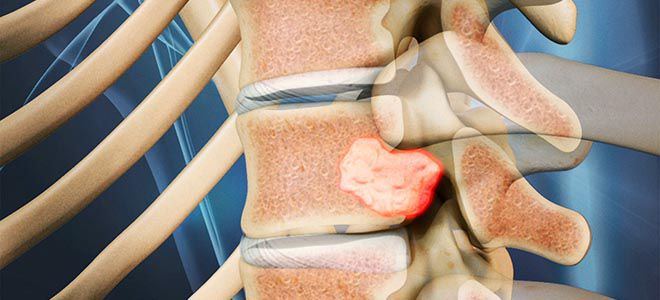
Осложнения миеломной болезни
Для множественной миеломы характерны осложнения, связанные с разрушающей деятельностью опухоли:
- сильные боли и разрушение костей (переломы);
- почечная недостаточность с необходимостью прохождения гемодиализа;
- постоянные инфекционные заболевания;
- анемия в серьезной стадии, требующая переливаний.
Анемия
Анемия является проявлением миеломной болезни примерно у 75% больных. Анемия обычно нормохромная и нормоцитарная, с признаками гипопролиферации (индекс ретикулоцитов < 2,5%), с повышенным уровнем ферритина (показатель воспаления). Число гипохромных эритроцитов >5% и низкое насыщение трансферрина типичны для дефицита железа. В этих случаях уровень анемии умеренный. Но у 10% больных с Hb< 80 г/л отмечается снижение качества жизни и неблагоприятный прогноз. Анемия редко обнаруживается у лиц с начальной болезнью. Уровень гемоглобина определяет время начала лечения анемии при миеломной болезни. Несколько факторов ответственны за развитие анемии. Это инфильтрация костного мозга миеломными клетками, приводящая к уменьшению числа эритроидных клеток-предшественников, дефицит эритропоэтина у больных с почечной недостаточностью, пониженный ответ проэритробластов на эритропоэтин почек, нарушенная утилизация железа вследствие высокого уровня гепсидина при хроническом воспалении, увеличенный объем плазмы при повышенном уровне парапротеинов, побочное действие терапии. Однако главной причиной анемии при миеломной болени является вызванный миеломными клетками апоптоз эритробластов.
При стойкой симптоматичной анемии и при уровне гемоглобина менее 100 г/л следует исключить вероятность других причин анемии (Fe-дефицитной, В12-дефицитной, гемолитической, хронических инфекций и т.д.). В случае железо-дефицитной анемии, которая устанавливается по числу гипохромных эритроцитов 5% и по пониженному уровню насыщения трансферина (ОЖСС) менее 20%, используются в/в препараты железа.
Уровень гемоглобина определяет время начала лечения анемии при миеломной болезни. Одними из методов предсказание эффекта эритпропоэз-стимулирующих агентов, в частности, эритропоэтинов является определение сохранности функции костного мозга. Так как тромбомодулин, стимулирующий тромбоцитоз, синтезируется преимущественно печенью, костно-мозговой ресурс сохранен при количестве тромбоцитов в крови более 150х10^9 кл/л. Исходно пониженный уровень эритропоэтина в крови важен для предсказания положительного ответа на терапию рекомбинантным эритропоэтином, что позволяет отказаться от переливания эритроцитарной массы. Частыми побочными эффектами использования эритропоэтинов являются тромбоэмболические осложнения и артериальная гипертензия.
Суть заболевания
Плазматические клетки вырабатывают иммунные антитела и представляют собой, по сути, лейкоциты, образованные из В-лимфоцитов. Они находятся в костном мозге, лимфоузлах, кишечнике и миндалинах. В норме количество плазмоцитов не превышает 5% от общего числа клеток костного мозга. Если эта цифра больше 10%, то можно говорить о развитии патологии.
Основной функцией плазматических клеток является синтез иммуноглобулинов для иммунной защиты в биологических жидкостях: крови, лимфе и слюне. Только за одну секунду ими производится несколько сотен антител-иммуноглобулинов.
Когда на одном из этапов созревания В-лимфоцитов происходит сбой, вместо плазматической образуется миеломная клетка, обладающая злокачественными свойствами. Свое название она получила в связи с тем, что патологический процесс развивается в основном в костном мозге.
Все другие миеломные клетки происходят из единственной мутировавшей клетки, которая активно размножалась. Их скопление носит название плазмоцитомы и может обнаруживаться в костях, мышцах.
Опухолевая клетка формируется в костном мозге и прорастает в кость, где начинает активно клонироваться. Их количество быстро растет, и патологические иммуноглобулины – парапротеины – проникают в кровь. Парапротеин не участвует в работе иммунитета, а откладывается в различных тканях. Поэтому его можно обнаружить в анализах крови.
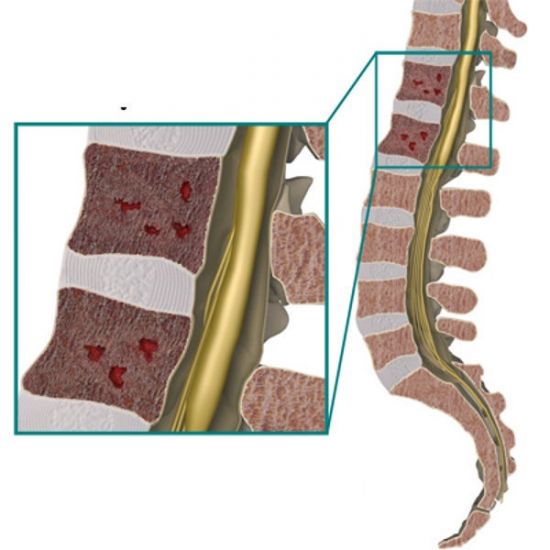 При миеломе в костях и позвонках образуются пустоты разной величины и локализации
При миеломе в костях и позвонках образуются пустоты разной величины и локализации
Находясь внутри костной ткани, злокачественные клетки стимулируют работу остеокластов, которые разрушают хрящи и кости, оставляя лишь пустоту на их месте. Кроме этого, они выделяют специфические информационные молекулы – цитокины. Данные вещества крайне негативно влияют на здоровье, поскольку:
- способствуют размножению миеломных клеток. Чем больше их становится, тем скорее образуются новые патологические очаги;
- подавляют функцию иммунной системы, которая не может бороться с опухолевыми клетками и остается беззащитной перед бактериальными инфекциями;
- стимулируют остеокласты – разрушители костной ткани. Кости слабеют и могут ломаться даже от незначительного воздействия;
- активизируют образование фибробластов, продуцирующих эластин и фибриноген. В результате кровь сгущается, на теле появляются синяки и кровоподтеки;
- вызывают рост гепатоцитов – печеночных клеток, из-за чего нарушается выработка протромбина и фибриногена, и ухудшается кровесвертывающая способность;
- изменяют белковый обмен, что приводит к повреждению почек. Особенно ярко этот симптом выражен при миеломе Бенс-Джонса.
Отек костного мозга позвоночника
Симптомы миеломной болезни
Симптомы:
- Боли в костях. Под воздействием миеломных клеток в кости образуются полости. Костная ткань богата болевыми рецепторами, при их раздражении развивается ноющая боль. Она становится сильной и острой при повреждении надкостницы.
- Боли в сердце, суставах, мышечных сухожильях связаны с отложением в них патологических белков. Эти вещества нарушают функционирование органов и раздражают чувствительные рецепторы.
- Патологические переломы. Под воздействием злокачественных клеток в кости образуются пустоты. Развивается остеопороз, кость становится хрупкой и ломается даже при незначительной нагрузке. Чаще всего происходят переломы бедренных костей, ребер и позвонков.
- Снижение иммунитета. Нарушается функция костного мозга: он вырабатывает недостаточно лейкоцитов, что приводит к угнетению защитных сил организма. Количество нормальных иммуноглобулинов в крови уменьшается. Часто возникают бактериальные инфекции: отит, ангина, бронхит. Болезни затяжные и плохо поддаются лечению.
- Гиперкальциемия. Из разрушенной костной ткани большое количество кальция попадает в кровь. Это сопровождается запорами, болью в животе, тошнотой, выделением большого количества мочи, эмоциональными расстройствами, слабостью, заторможенностью.
- Нарушение функции почек – миеломная нефропатия вызвана тем, что кальций откладывается в почечных протоках в виде камней. Также почки страдают от нарушения белкового обмена. Парапротеины (белки, вырабатываемые раковыми клетками) поступают через почечный фильтр, и откладывается в канальцах нефронов. При этом почка сморщивается (нефросклероз). Кроме того нарушается отток мочи из почек. Жидкость застаивается в почечных чашечках и лоханках, при этом атрофируется паренхима органа. При миеломной нефропатии отеки отсутствуют, артериальное давление не повышено.
- Анемия, преимущественно нормохромная – цветовой показатель (соотношение гемоглобина к количеству эритроцитов) остается в норме 0,8 -1,05. При повреждении костного мозга снижается выработка эритроцитов. При этом пропорционально уменьшается концентрация гемоглобина в крови. Поскольку гемоглобин отвечает за транспортировку кислорода, то при анемии клетки ощущают кислородное голодание. Это проявляется быстрой утомляемостью, снижением концентрации внимания. При нагрузке возникает одышка, сердцебиение, головная боль, бледность кожи.
- Нарушения свертываемости крови. Повышается вязкость плазмы. Это приводит к спонтанному склеиванию эритроцитов в виде монетных столбиков, что может вызвать образование тромбов. Снижение уровня тромбоцитов (тромбоцитопения) приводит к спонтанным кровотечениям: носовым и десенным. Если повреждаются мелкие капилляры, то кровь выходит под кожу – образуются синяки и кровоподтеки.