Генетический анализ на рак
Содержание:
- В моей семье были случаи рака молочной железы. Можно определить грозит ли мне наследственная форма РМЖ?
- Для кого это исследование
- Мы все — мутанты, это норма. Но некоторые мутации приводят к раку
- Показания
- Интересные факты и статистика:
- Почему нужно проверять такое большое количество показателей, если вид моего рака уже известен?
- Какой анализ можно сделать вместо теста на онкомаркеры?
- Как проводят диагностику?
- Как делают генетическое тестирование на рак?
- Каждый рак уникален
- Группы риска
- Что делать здоровым носительницам мутаций?
- Список исследований, доказанно снижающих смертность от рака
- График работы поликлиник на весь период проведения программы
- Опухоли и специфика генетических тестов
- Для кого это исследование
- Как выглядит заключение
- Как выглядит заключение
В моей семье были случаи рака молочной железы. Можно определить грозит ли мне наследственная форма РМЖ?
Да, можно. Для этого надо сдать генетический анализ в диагностической лаборатории. У вас возьмут образец венозной крови или соскоб со слизистой щеки и с помощью методов молекулярной диагностики изучат генетический материал ваших клеток. Если мутация есть, то результат анализа будет положителен. Однако тест рекомендуют проводить не всем людям, имеющим родственников с РМЖ. Основанием для назначения анализа здоровым женщинам служат следующие условия:
- двое и более ваших родственников болели раком груди, включая мужчин (отец, брат, дед);
- даже одному вашему родственнику диагноза РМЖ или рака яичников был поставлен ранее 40 лет;
- в вашей семье были случаи рака сразу обеих молочных желез;
- ваш возраст старше 20 лет.
Для кого это исследование
Применение этого исследования показано следующим группам обследуемых:
Здоровым людям с семейной историей онкологических заболеваний (например, при наличии трёх и более случаев рака молочной железы в семье в одной линии);
Здоровым людям без онкологических заболеваний в семье тест может дать важную информацию о генетической предрасположенности к онкологическим заболеваниям, поскольку человек может быть носителем новых мутаций, которых нет у родителей, и кроме того, наследственный рак может наследоваться от здоровых носителей мутаций. При этом в семье может не быть случаев рака, но у данного конкретного пациента будет присутствовать новая комбинация онкогенных мутаций, унаследованная от обоих родителей — носителей, вызывающая рак.
Пациентам с диагностированным раком в случае подозрения на наследственную природу, например,
- в случае относительно раннего возраста развития рака,
- в случае отягощённого семейного анамнеза,
- при определённых типах опухолей (например, опухоли толстой кишки с высокой микросателлитной нестабильностью),
- при наличии двух и более первичных очагов опухоли (например, билатеральный рак молочной железы), либо нескольких первичных типов рака у одного пациента.
У этой группы пациентов поиск мутации может быть необходим для выбора тактики лечения и назначения определённой таргетной терапии (например, в случае наличия мутаций в генах BRCA 1/2 может быть назначен препарат олапариб). Таргетная терапия блокирует рост клеток опухоли, прицельно нарушая механизм действия конкретных молекул, необходимых для жизнедеятельности опухоли.
Конечная цель исследования – полная информация о мутациях, связанных с наследственными формами рака, интерпретированная специалистом с точки зрения клинической значимости.
Мы все — мутанты, это норма. Но некоторые мутации приводят к раку
«Порядочные» клетки живут, не мешая другим. Используют строго отведенное количество ресурсов, достойно выполняют свои биологические функции, а в положенное время — умирают, уступая место следующим поколениям (этот процесс называется апоптозом). Каждые 7–10 лет тело человека полностью обновляется.
Для этого все соматические клетки (те, из которых состоит организм), кроме эритроцитов, беспрестанно делятся.
Перед делением клетка запасается «копией» наследственной генетической информации, которая находится в ее ядре. Нити ДНК, «свернутые» в хромосомы внутри ядра — реплицируются, т. е. удваиваются. И уже после этого клетка делится, спокойно раздавая каждой из дочерних клеток по идентичному набору хромосом. Из одной клетки получается две абсолютно таких же, и вместе со своим генетическим багажом каждая из них получает «знания» о том, как ей надо жить, какую функцию выполнять и сколько раз в жизни делиться.

Иногда в процессе деления получаются сбои — мутации. То нить ДНК порвется, то скопируется с ошибкой, то участки хромосом перемешаются. Влиять на это может сотня факторов: от стресса и табачного дыма до воздействия радиации.
Показания
Сегодня генетический анализ на рак позволяет выявить риск развития онкопатологий:
- молочной железы;
- яичников;
- шейки матки;
- простаты;
- легких;
- кишечника и толстой кишки в частности.
Также, существует генетическая диагностика на некоторые врожденные синдромы, существование которых повышает вероятность развития рака нескольких органов. Например, синдром Ли-Фраумени говорит о риске рака мозга, надпочечников, поджелудочной железы и крови, а синдром Пейтца-Егерса говорит о вероятности онкопатологий пищеварительной системы (пищевод, желудок, кишечник, печень, поджелудочная железа).
Интересные факты и статистика:
- Мутация гена BRCA1 случается чаще, чем мутация BRCA2.
- У носителей BRCA1-мутаций, страдающих РМЖ, риск возникновения рака второй молочной железы в 1,6 раза выше, чем у носителей BRCA2-мутаций.
- Среднестатистический риск развития рака молочной железы составляет 12%, а при мутации генов BRCA1 и BRCA2 риск возрастает до 40%-85%.
- Риск развития рака яичников также возрастает с 2% до 16-44%.
- Молодой возраст (до 35 лет) на момент выявления первой опухоли связан с более высоким риском развития рака второй молочной железы у пациенток с мутацией в гене BRCA1.
- Наследование двух аномальных копий генов BRCA2, BRIP1, MRE11A, NBN, PALB2, RAD50 и RAD51C вызывает анемию Фанкони, которая приводит к угнетению всех ростков кроветворения.
- В России при РМЖ помимо мутации генов BRCA1 и BRCA2, распространена мутация гена CHEK2 (не менее 2%).
Почему нужно проверять такое большое количество показателей, если вид моего рака уже известен?

Из-за большого количества больных, китайские специалисты – онкологи традиционно пошли дальше своих коллег из других стран в развитии и применении таргетной терапии.
Исследования таргетной терапии в различных вариациях ее применения привели к интересным результатам. Разные таргетные препараты действуют на соответствующие мутации генов. Но сами генные мутации, как оказалось, далеко не так жестко привязаны к определеному виду рака.
Например, у пациента с раком печени после проведения полного комплекса генетических анализов была выявлена мутация, при которой высокий эффект показывает препарат Иресса, предназначенный для рака легкого. Лечение этого пациента препаратом для рака легкого привело к регрессу опухоли печени! Этот и другие подобные случаи придали совершенно новый смысл определению генетических мутаций.
В настоящее время проверка полного комплекса генетических анализов позволяет расширить список препаратов таргетной терапии теми лекарствами, которые изначально не предусматривались для использования, что существенно увеличивает клиническую эффективность лечения.
Генетические анализы определяются по тканям опухоли (это предпочтительнее! подойдет опухолевый материал после операции или после пункционной биопсии) или по крови (кровь из вены).
Для более точного определения генных мутаций, особенно при рецидивах, рекомендуется проводить повторную биопсию с забором нового опухолевого материала. Если биопсия практически невозможна или рискованна, тогда анализ проводят по венозной крови.
Результат готов через 7 дней. Заключение содержит не только результат, но и конкретные рекомендации с названиями подходящих препаратов.
Какой анализ можно сделать вместо теста на онкомаркеры?
Если вы очень боитесь заболеть раком, то стоит не только сдавать анализы, но и пообщаться с психотерапевтом. Навязчивые мысли о раке у здорового человека могут говорить о канцерофобии.
Но если ваши подозрения не безосновательны (например, плохая наследственность), то стоит пройти генетическое тестирование. Например, такое исследование проходила Анджелина Джоли. Она приняла решение о профилактической операции (у актрисы удалены молочные железы и яичники), когда выяснила, что ее близкие родственницы умерли от рака груди и яичников.
Самые распространённые виды рака у женщин — это рак молочной железы и яичников, который выявляют анализы на мутации в генах BRCA1 и BRCA2 . У мужчин это анализ на PSA (общий простатический специфический антиген), указывающий на рак предстательной железы. Кстати, последние исследования показали, что уровень ПСА не всегда служит надежным основанием для начала диагностических мероприятий. Поэтому сейчас врачи рекомендуют сдавать ПСА только после консультации с урологом.
Также можно сделать генетические тесты на мутации генов, которые вызывают колоректальный рак, меланому, рак лёгкого, и оценить разные факторы риска с точки зрения генетической предрасположенности. Например, риск развития онкологического заболевания при курении или употреблении жареных и копчёных продуктов.
Как проводят диагностику?
Генетическое тестирование проходит в два этапа:
- 1. Родственник, больной раком сдает кровь для диагностики, чтобы определить, есть ли у него ген, вызывающий рак (это нужно сделать до тестирования любого здорового родственника). Результат будет готов через 6-8 недель.
- 2. Если результат анализа крови вашего родственника положительный, вы можете проходить предиктивное генетическое тестирование, чтобы определить, есть ли у вас такой же мутировавший ген. Ваш врач направит вас в местную службу генетических исследований, где у вас возьмут кровь (возьмите с собой копию результатов анализов вашего родственника). Результаты будут готовы максимум через 10 дней после того, как у вас возьмут кровь, но скорее всего, это произойдет не во время первого приема.
Благотворительная организация Breakthrough Breast Cancer объясняет важность этих двух шагов: «Без предварительного анализа генов заболевшего родственника тестирование здорового человека будет напоминать чтение книги, когда ищешь в ней опечатку и не знаешь, где она и есть ли она там вообще»
Как делают генетическое тестирование на рак?
Перед генетическим тестированием на повышенный риск развития рака обязательно выполняют несколько шагов для определения стоит ли делать столь дорогое исследование. Такими шагами являются:
- Оценка риска, т.е. есть ли вообще вероятность того, что вы заболеете определенным видом онкологии. Это основано на личной и семейной истории болезни.
- Генетическая консультация. Перед прохождением генетического тестирования вам необходимо будет сходить на консультацию к специально обученному медицинскому работнику. Он подскажет какие результаты и последствия могут быть из-за тестирования. На этом этапе вы вполне можете отказаться от исследования или, наоборот, заказать тестирование сразу для нескольких членов семьи.
- Информационное согласие. Это обязательный этап перед сдачей анализа. Нужно дать согласие на исследование в письменной форме. Возможно, придется заполнить достаточно подробную анкету, включающую причины, побудившие на прохождение тестирования, и планируемые дальнейшие варианты использования полученных данных.
Дальнейшие действия, фактически само генетическое тестирование на рак, выполняется только после прохождения предыдущих шагов:
- Сбор образцов и лабораторные тестирования. Для исследования на наличие мутирующих генов, повышающих риск развития рака, необходимо несколько труб крови из вены.
- Получение результатов тестирования. Результаты тестирования пересылают генетическому консультанту. Это делается для того, чтобы пациент смог лучше в них разобраться и понять, что делать дальше, так как генетический тест не всегда дает однозначные ответы. В некоторых случаях результатов приходится ждать недели и даже месяцы
Каждый рак уникален
Еще совсем недавно злокачественные опухоли классифицировали только по гистологическому принципу, то есть в зависимости от того, в каком органе они возникали, и как опухолевая ткань выглядела под микроскопом.
С развитием молекулярной биологии и генетики, ученые смогли заглянуть глубже. Изучены многие мутации, приводящие к раку, «неправильные» молекулы, благодаря которым опухоль бесконтрольно растет, поддерживает свою жизнедеятельность, защищается от иммунной системы. Заблокировать эти молекулы и тем самым затормозить прогрессирование заболевания помогают современные таргетные препараты, иммунопрепараты.
Сложность в том, что не существует двух злокачественных опухолей с одинаковыми молекулярно-генетическими характеристиками. Набор мутаций всегда разный, поэтому универсальной «таблетки от рака» нет и быть не может. Для того чтобы назначить эффективное лечение, врач должен понимать, какие мутации есть в опухолевых клетках у конкретного пациента, присутствуют ли в них «мишени» для того или иного препарата.
Для этого и нужны молекулярно-генетические анализы.
Некоторые из генов, связанных с развитием рака, хорошо изучены и постоянно на слуху. Например это мутации EGFR при раке легких, HER2, BRCA1 и BRCA2 при раке молочной железы, BRAF при меланоме.
Американская компания Foundation Medicine, Inc. (Кембридж, США) проводит комплексное генетическое профилирование, во время которого изучают все известные мутации четырех разных классов более чем в 300 генах. Это помогает составить максимально полный «молекулярный портрет» злокачественной опухоли и выбрать наилучшую схему лечения.
В конце 2018 года швейцарская компания Roche наладила доставку биоматериала от онкологических пациентов из России в лабораторию Германии, где есть возможность провести такой анализ. Транспортировка биоматериала проводится в соответствии со всеми требованиями Росздравнадзора.
Мы в Европейской клинике поддерживаем это начинание и считаем его важным шагом в развитии помощи онкологическим больным в России. Если пациенту необходим молекулярно-генетический анализ, наши врачи рассказывают о такой возможности и помогают ею воспользоваться.
Группы риска
В группы риска по наследственному раку попадают люди, у которых наблюдается хотя бы один из перечисленных факторов:
- Несколько случаев одного вида рака в семье(например, рак желудка у деда, отца и сына);
- Заболевания в раннем для данного показания возрасте(например, колоректальный рак у пациента моложе 50 лет);
- Единичный случай определенного вида рака(например, рак яичников, или трижды негативный рак молочной железы);
- Рак в каждом из парных органов(например, рак левой и правой почки);
- Больше одного типа рака у родственника(например, сочетание рака молочной железы и рака яичников);
- Рак, нехарактерный для пола пациента(например, рак молочной железы у мужчины).
Если для человека и его семьи характерен хотя бы один фактор из списка, то следует получить консультацию у врача-генетика. Он определит, есть ли медицинские показания для того, чтобы сдавать генетический тест.
Чтобы обнаружить рак на ранней стадии, носителям наследственного опухолевого синдрома следует проходить тщательный скрининг на онкологические заболевания. В некоторых случаях риск развития рака можно существенно снизить с помощью превентивных операций и лекарственной профилактики.
Генетический «вид» раковой клетки в процессе развития изменяется и теряет свой первоначальный вид. Поэтому, чтобы использовать молекулярные особенности рака для лечения, недостаточно исследовать только наследственные мутации. Для выявления слабых мест опухоли нужно провести молекулярное тестирование образцов, полученных в результате биопсии или операции.
При проведении теста опухоль анализируется, составляется индивидуальный молекулярный паспорт. В комплексе с анализом крови, в зависимости от требуемого теста, проводится комбинацирование различных анализов на геном и белок. В результате данного теста появляется возможность назначения таргетной терапии, эффективной для каждого типа имеющейся опухоли.
Что делать здоровым носительницам мутаций?
- Обследование молочных желёз у маммолога начиная с 25 лет раз в 6 месяцев
- Маммография с 25 лет раз в 6-12 месяцев
- Магнитно-резонансная томография грудной клетки с 25 лет раз в 6-12 месяцев
- Самообследование молочных желёз с 18 лет ежемесячно
- Профилактическая мастэктомия после 35 лет, разрешенная в Европе, однако не проводится в Российской Федерации
- Профилактическая овариэктомия после 40 лет, также разрешенная в Европе, однако не проводится в Российской Федерации без доказательства наличия патологических клеток
- Регулярная сдача анализа на онкомаркер СА125
Пройти генетическое тестирование или записаться на консультацию к врачу-генетику и получить всю необходимю информацию в Москве можно в Центре семейной генетики FG Lab (Family genetics laboratory).
Список исследований, доказанно снижающих смертность от рака
(по данным National Cancer Institute, США)
Колоноскопия, сигмоидоскопия и высокочувствительные методы обнаружения крови в кале — для рака толстой кишки. При проведении колоноскопии и сигмоидоскопии врач имеет возможность обнаружить полипы кишечника и удалить их до того, как они переродятся в раковую опухоль. Обычно проведение в качестве скрининга эндоскопических исследований кишечника рекомендуется в возрасте от 50 до 70 лет.
Низкодозированную спиральную томографию легких применяют в качестве скринингового обследования у тяжелых курильщиков в возрасте от 55 до 74 лет.
Маммографию проводят у женщин в возрасте от 40 до 74 лет для раннего выявления рака молочной железы. Метод существенно снижает смертность от этого заболевания, особенно в группе старше 50 лет.
Пап-тест и анализы на вирус папилломы человека снижают заболеваемость раком шейки матки, так как обнаруживают атипичные клетки до развития опухоли. Смертность от этой патологии неуклонно снижается. Эти исследования рекомендуют проводить регулярно, начиная с 21 года и до 64 лет.
Другие скрининговые тесты
Определение альфа-фетопротеина в крови совместно с УЗИ печени применяют в качестве скрининга рака печени при высоком риске его развития.
МРТ молочных желез используют при мутациях в генах BRCA1 или BRCA2. У этой группы очень высок риск рака груди и некоторых других злокачественных новообразований.
Определение онкомаркера CA-125 в крови часто делают вместе с трансвагинальным УЗИ женских половых органов для раннего обнаружения рака яичников, особенно при повышенном риске этого заболевания.
Самообследование молочных желез и врачебный осмотр груди не снижают смертность от рака молочной железы. Конечно, при обнаружении образования в молочной железе необходимо полное обследование для постановки диагноза.
Анализ крови на маркер ПСА совместно с пальцевым ректальным исследованием предстательной железы позволяет обнаружить опухоль простаты на ранней стадии.
Регулярно проводить осмотр кожи часто рекомендуют людям с высоким риском рака кожи. Хотя такое самообследование не снижает смертность от злокачественных новообразований кожи и приводит иногда к гипердиагностике, изменения формы и цвета родинок, появление новых или изъязвлений на коже — повод обратиться к врачу.
Трансвагинальное УЗИ позволяет получить изображение яичников и матки, что важно для женщин с повышенным риском рака яичника (с мутацией BRCA1 или BRCA2 ) или рака эндометрия (с синдромом Линча). Раннее выявление злокачественных опухолей очень важно для снижения смертности, а при выявлении предрака — и заболеваемости
Раннее выявление злокачественных опухолей очень важно для снижения смертности, а при выявлении предрака — и заболеваемости
График работы поликлиник на весь период проведения программы
«За четыре субботы в наши поликлиники пришли 16 тысяч женщин и порядка четырех тысяч мужчин. Традиционно женщины более активно участвуют в программе. Мы призываем мужчин также заботиться о своем здоровье и использовать возможность сделать анализ быстро и рядом с домом
Важно отметить, что выявление злокачественных опухолей на начальных стадиях позволяет в большинстве случаев вылечить заболевание полностью. Программу по ранней диагностике рака “Я выбираю здоровое будущее!” мы специально проводим по субботам с 08:00, чтобы все желающие смогли прийти и сдать кровь на анализ
Вся процедура занимает не более 30 минут. Предварительная запись и направление врача не требуются», — сообщил глава столичного Департамента здравоохранения Алексей Хрипун.
У женщин на предрасположенность к раку молочной железы и яичников указывает наличие мутаций генов BRCA1 и BRCA2. На признаки рака предстательной железы у мужчин — повышенный уровень ПСА (простатического специфического антигена).

Жители столицы могут выбрать любые удобные дату и место для проведения обследования. Результаты анализов обрабатываются приблизительно полтора месяца. Их можно получить по электронной почте либо в поликлинике по месту прикрепления. Если исследования покажут отклонения от нормы, мужчин пригласят на консультацию в поликлинику, а женщин — в клинику женского здоровья Московского клинического научного центра имени А.С. Логинова. Вся информация строго конфиденциальна.
Проект «Я выбираю здоровое будущее!», направленный на раннюю диагностику онкозаболеваний, впервые был запущен в марте этого года. Тогда за два дня, 17 и 18 марта, бесплатное обследование в 10 столичных поликлиниках прошли около 16 тысяч человек — 3361 мужчина и порядка 12 тысяч женщин.
По результатам онкоскрининга рак предстательной железы был диагностирован у 47 мужчин (у 39 из них на ранней стадии). 45 мужчинам уже назначено лечение, а 17 человек успешно прооперированы.
Мутации гена BRCA, которые могут спровоцировать рак молочной железы и яичников, выявлены у 43 женщин. Их направили в клинику женского здоровья Московского клинического научного центра имени А.С. Логинова. 20 пациенток уже получили медицинскую консультацию. В двух случаях был диагностирован рак молочной железы. Сейчас женщины проходят необходимое лечение.
Опухоли и специфика генетических тестов
Информация, хранящаяся в наших генах, определяет характеристики каждого человека, например, такие как группа крови и цвет глаз. С генами также передаются генетические заболевания, которые мы наследуем от наших родителей или более ранних поколений, и предрасположенность к определенным болезням, например, к раку.
Сам рак не передается от родителей к детям. Однако, если в ДНК потомства обнаружены мутированные гены, вероятность развития рака значительно возрастает.
Мутированный ген
Генетические тесты, проводимые на рак, включают анализ определенных генов, которые могут быть ответственны за развитие определенного типа рака. Часто рак, от которого пострадал член семьи, является показателем риска, который важен для здоровья других родственников. Вот почему генетическое тестирование рекомендуется людям, у которых в семье были опухоли, особенно злокачественные или многоорганные.
Образцы, используемые для проведения генетических тестов, обычно представляют собой кровь из вены на руке или слюну.
Генетические тесты на рак молочной железы и яичников
Один из наиболее распространенных видов рака у женщин — рак молочной железы и яичников. Чаще всего он развивается после 50 лет, хотя заниматься профилактикой рака молочной железы нужно гораздо раньше. Проходить регулярные обследования молочных желез и яичников, делая УЗИ молочных желез и трансвагинальное УЗИ, нужно, начиная с 25-30 лет. После 45 лет ежегодно проводится маммография.
Маммография
Но самую точную и раннюю информацию по рискам рака мы можем получить абсолютно в любом возрасте на основе генетического тестирования. Сделать такой анализ нужно как можно раньше.
Если в семье есть случаи рака груди и яичников или других видов рака, генетические тесты покажут, унаследовала ли женщина опасные мутации. Если это так, медицинские осмотры следует начинать еще до 25 лет.
Большая предрасположенность к развитию рака молочной железы и яичников проявляется в основном в случае мутаций в генах BRCA1 и BRCA2, иногда также рассматриваются CHEK2, NBS или NOD2.
Генетические тесты на рак простаты
Рак предстательной железы распространен среди мужчин старше 50 лет. Если опухоль обнаружена поздно, в большинстве случаев это связано с плохим прогнозом. Вот почему мужчины, в том числе молодые люди, которым грозит опасность из-за плохой наследственности, должны обязательно пройти генетическое тестирование.
Рак простаты
Ранняя диагностика рака предстательной железы имеет решающее значение в его лечении. Симптомы этого заболевания не очень характерны, поэтому ДНК-тесты помогут определить, не являются ли их основной причиной раковые поражения. На рак предстательной железы влияет мутация генов CHECK2, HOXB13, NBS1 и BRCA1.
Для кого это исследование
Применение этой панели показано следующим группам:
Здоровым женщинам с семейной историей онкологических заболеваний (например, при наличии трёх и более случаев рака молочной железы в семье в одной линии).
Здоровым женщинам без семейной истории онкологических поражений этих органов тест может дать важную информацию о генетической предрасположенности к онкологическим заболеваниям такого профиля, поскольку человек может быть носителем новых мутаций, которых нет у родителей. Кроме того, наследственный рак может наследоваться от здоровых носителей мутаций. При этом ранее в семье могло не быть случаев рака, но у данной конкретной пациентки будет присутствовать новая комбинация онкогенных мутаций, унаследованных от обоих родителей-носителей, которая может вызвать рак.
Пациенткам с диагностированным раком молочной железы или яичников в случае подозрения на наследственную природу заболевания, например,
- в случае отягощённого семейного анамнеза,
- в случае относительно раннего (до 45 лет) возраста развития рака,
- всем пациенткам с раком яичников,
- при определённых типах опухолей молочной железы (например, пациенткам моложе 60 лет с тройным негативным фенотипом),
- при наличии двух и более первичных очагов опухоли (например, опухоли обеих молочных желёз) либо нескольких первичных типов рака (например, рак молочной железы и рак поджелудочной железы) у одной пациентки,
- беременным пациенткам,
- пациентам-мужчинам с раком молочной железы.
У этой группы пациентов поиск мутации может быть необходим для выбора тактики лечения и назначения определённой таргетной терапии (например, в случае наличия мутаций в генах BRCA 1/2 может быть назначен препарат олапариб). Таргетная терапия направленно блокирует рост клеток опухоли, прицельно нарушая реализацию действия конкретных молекул, необходимых для опухолевого роста и развития онкологического процесса.
Конечная цель исследования – полная информация о мутациях, связанных с наследственными формами рака молочной железы и яичников, интерпретированная специалистом с точки зрения клинической значимости.
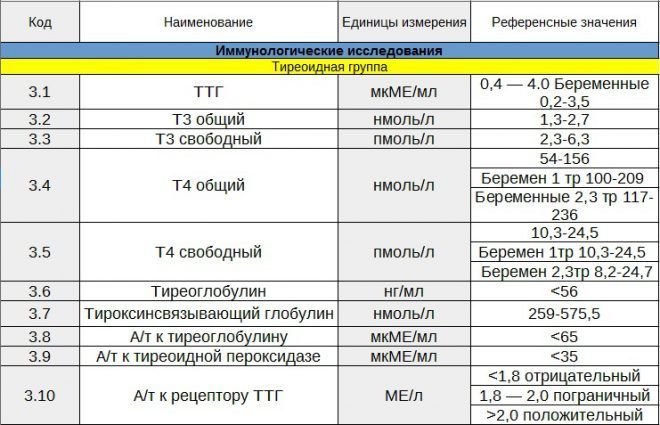
Как выглядит заключение
Заключение содержит описание результатов исследования и представляет их следующим образом:
- в случае здорового человека – список патогенных и вероятно патогенных мутаций, их описание и интерпретация. Мутации с неизвестным клиническим значением в заключение не выносятся в связи с серьёзными сложностями их дальнейшей клинической интерпретации у здорового человека и низкой информативностью для дальнейших диагностических мероприятий.
- в случае пациентов с диагностированным раком – список патогенных, вероятно патогенных мутаций и мутаций с неизвестным клиническим значением, их описание и интерпретация.
Заключение отправляется заказчику исследования по электронной почте. Если есть необходимость получить заключение в бумажном варианте, мы отправим его в любой регион почтой России без дополнительных расходов для заказчика.
Как выглядит заключение
Формат заключения включает в себя описание результатов исследования и выглядит следующим образом:
в случае здорового человека — список патогенных и вероятно патогенных мутаций, их описание и интерпретация. Мутации с неизвестным клиническим значением в заключение не выносятся в связи с серьёзными сложностями их дальнейшей клинической интерпретации у здорового человека и низкой информативностью для дальнейших мероприятий.
в случае пациентов с диагностированным раком — список патогенных, вероятно патогенных мутаций и мутаций с неизвестным клиническим значением, их описание и интерпретация.
Заключение отправляется заказчику по электронной почте. Если есть необходимость получить заключение на бумаге, мы отправим его в любой регион почтой России. Это входит в стоимость.